Error. No debería verse este texto.
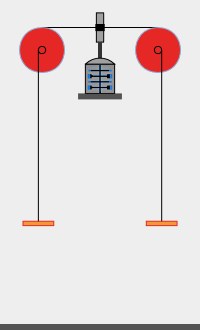 En un aparato de Joule se calientan 50 gramos de agua al dejar caer dos pesas de 15 kg de masa desde una altura de 19 metros. ¿Cuánto aumentará la temperatura del agua? El calor específico del agua es 4180 J·kg-1·K-1 y la gravedad es 9,8 m/s2.
El aparato de Joule es un sistema adiabático, es decir, no hay transferencia de calor entre el líquido y el exterior. Por lo tanto, la variación de energía interna ΔU se debe únicamente al trabajo W transferido, que en este caso procede de la diferencia de energía potencial:
En un aparato de Joule se calientan 50 gramos de agua al dejar caer dos pesas de 15 kg de masa desde una altura de 19 metros. ¿Cuánto aumentará la temperatura del agua? El calor específico del agua es 4180 J·kg-1·K-1 y la gravedad es 9,8 m/s2.
El aparato de Joule es un sistema adiabático, es decir, no hay transferencia de calor entre el líquido y el exterior. Por lo tanto, la variación de energía interna ΔU se debe únicamente al trabajo W transferido, que en este caso procede de la diferencia de energía potencial:
ΔU = -W = -ΔEp
Indica el aumento de temperatura en el apartado Test.
Título resultado
En el aparato de Joule la variación de energía interna ΔU se debe únicamente al trabajo W transferido, que procede de la diferencia de energía potencial y que actúa igual que una fuente de calor:
ΔU = -W = -ΔEp = Q -mpesa · g · (hf - hi) = magua · cv · ΔT -19 · 9,8 · (0 - 10) = 0,05 · 4180 · ΔT ΔT = 10 K
Pulsa el botón Enviar y entra en el siguiente ejercicio.
No has indicado un valor para la variación de temperatura. No puede ser cero.
Has gastado un intento porque el valor que has indicado es incorrecto. Lee de nuevo el enunciado y revisa tus cálculos antes de volver a responder. Convierte todas las unidades al Sistema Internacional.